| 是否进驻政务大厅 | 是 | ||
| 办理地点 | 苏州市政务服务中心:苏州市平泷路251号3楼市场监管局综合窗口E34窗口 | ||
| 办理时间 | 周一至周六上午:09:00~12:00 ,下午:13:00~17:00,法定节假日除外 。 | ||
| 序号 | 材料名称 | 表格下载 | 来源渠道 | 纸质材料 | 材料必要性 | 填报须知 | 详情 |
|---|---|---|---|---|---|---|---|
| 1 |
接受使用单位委托代理进口的,还需提供委托代理协议复印件和进口单位的《企业法人营业执照》、《进出口企业资格证书》(或《对外贸易经营者备案登记表》)、《组织代码证书》复印件。(教学科研、境外委托生产) |
申请人自备 | 1份 | 必要 | 查看更多 | ||
| 2 |
相应科研项目的批准文件或相应主管部门的批准文件(教学科研) |
申请人自备 | 1份 | 必要 | 查看更多 | ||
| 3 |
国内使用单位合法资质的证明文件、药品使用数量的测算依据以及使用单位出具的合法使用和管理该药品的保证函(教学科研、境外委托生产) |
申请人自备 | 1份 | 必要 | 查看更多 | ||
| 4 |
《进口药品注册证》(或者《医药产品注册证》)持有者如委托非本公司代理出口其药品的,需提供委托出口函(供临床用) |
政府部门核发 | 1份 | 必要 | 查看更多 | ||
| 5 |
进口单位的《药品经营许可证》、《企业法人营业执照》、《进出口企业资格证书》(或《对外贸易经营者备案登记表》)、《组织代码证书》复印件;药品生产企业进口本企业所需原料药和制剂中间体(包括境内分包装用制剂),应当报送《药品生产许可证》、《企业法人营业执照》、《组织代码证书》复印件;(供临床用) |
政府部门核发 | 1份 | 必要 | 查看更多 | ||
| 6 |
《进口药品注册证》(或者《医药产品注册证》)(正本或者副本)复印件(供临床用) |
政府部门核发 | 1份 | 必要 | 查看更多 | ||
| 7 |
购货合同或者订单复印件(供临床用、教学科研) |
申请人自备 | 1份 | 必要 | 查看更多 | ||
| 8 | 空白表格示例样表 | 申请人自备 | 1份 | 必要 | 查看更多 |
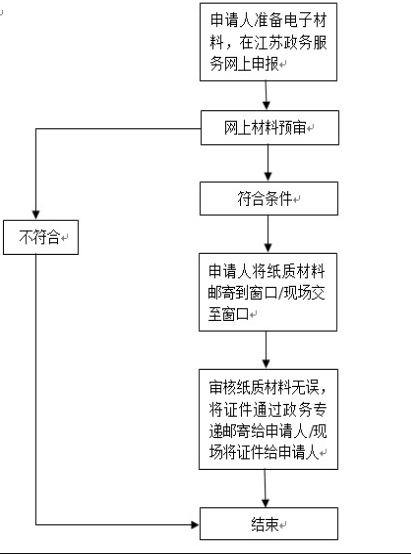
| 办件类型 | 承诺件 | ||
| 法定办结时限 | 20个工作日 | 承诺办结时限 | 5个工作日 |
| 法定办结时限说明 | 法定办结时限。 | 承诺办结时限说明 | 优化营商环境。 |
| 审批结果类型 | 证照 | 审批结果名称 | 药品进口准许证 |
| 审批结果样本 | 药品进口准许证 | ||
法律依据
《反兴奋剂条例》(2004年1月13日国务院令第398号,2014年7月29日予以修改)第十一条:进口蛋白同化制剂、肽类激素,除依照药品管理法及其实施条例的规定取得国务院食品药品监督管理部门发给的进口药品注册证书外,还应当取得省、自治区、直辖市人民政府食品药品监督管理部门颁发的进口准许证。申请进口蛋白同化制剂、肽类激素,应当说明其用途。省、自治区、直辖市人民政府食品药品监督管理部门应当自收到申请之日起15个工作日内作出决定;对用途合法的,应当予以批准,发给进口准许证。海关凭进口准许证放行。第十二条:申请出口蛋白同化制剂、肽类激素,应当说明供应对象并提交进口国政府主管部门的相关证明文件等资料。省、自治区、直辖市人民政府食品药品监督管理部门应当自收到申请之日起15个工作日内作出决定;提交进口国政府主管部门的相关证明文件等资料的,应当予以批准,发给出口准许证。海关凭出口准许证放行。
省政府关于公布企业投资项目省级部门不再审批事项清单(第二批)的决定 (苏政发〔2018〕33号) 第39项 蛋白质同化制剂、肽类激素进口准许证核发委托设区市食品药品监督管理部门实施。